Novinky
V rámci optimalizace instrumentační metody na Synapt G2 TOF jsme v posledních dnech udělali několik vylepšení.
- Snížení energie aplikované na ionty při přechodu ze zdroje do vakua (nově standardně nižší Cone Voltage, Extraction Cone Voltage, teplota desolvačního plynu a napětí na sprejovací kapiláře), pro omezení fragmentace proteinů v plynné fázi
- Zjištění limitu detekce na modelovém proteinu, úprava našeho interního QC na 5x nižší množství proteinu, úprava doporučeného minimálního množství vzorku z μg/μl na molaritu (dává větší smysl v rámci MS), ve výsledku na 20 μl proteinu o koncentraci 1 μM (podle velikosti proteinu 30x-5x nižší než současné doporučení)
Za poslední rok a půl jsme provedli téměř 2000 měření intaktní hmoty proteinů. Vzhledem k dobře fungující rutině a obecné spokojenosti uživatelů jsme neměli potřebu výrazně optimalizovat nastřikované množství proteinů. Nicméně poslední dobou jsme se několikrát setkali s požadavkem na analýzu méně koncentrovaného vzorku, než který jsme doporučovali a zjistili jsme, že někdo kvůli tomu k analýze ani nepřistoupil a neoslovil nás.
Prozkoumali jsme proto důkladně historicky používané množství proteinů v intaktní analýze, prozkoumali skutečnou citlivost našeho LC-MS systému a upravili náš QC standard. Výsledek je, že doporučované množství proteinu pro intaktní analýzu je nyní výrazně nižší. Budeme snižovat nastřikované množství proteinů na cca 5 pmol, což může znamenat až 30x nižší koncentraci, podle velikosti analyzovaných proteinů. Do teď jsme také uvažovali a doporučovali množství vzorků v μg/μl, což není pro MS praktické. Náš signál je závislý na fyzickém množství molekul v roztoku a tomu odpovídá jedině molarita roztoku. Pro větší proteiny bude tedy identický požadavek na 1 μM vzorek v μg/μl vždy vyšší, než pro malý protein.
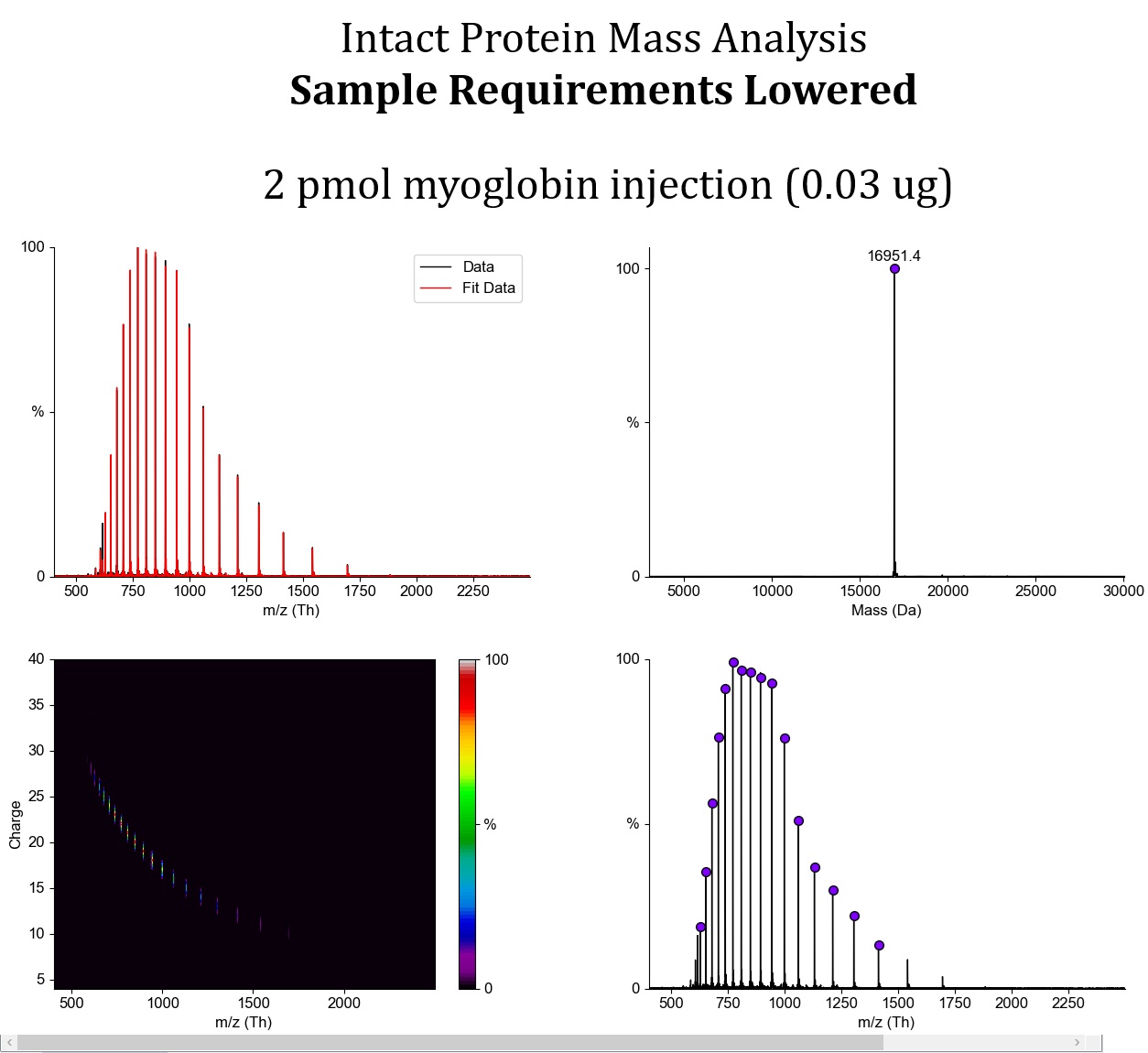
Také jsme si všimli, že některé proteiny našich uživatelů byly výrazně náchylnější na fragmentaci v plynné fázi, než jiné. Plošně proto snižujeme energii iontů při přechodu ze zdroje do hmotnostního spektrometru, abychom se vyhnuli jejich fragmentaci. Na modelovém myoglobinu jsme v zásadě kompletně eliminovali jakékoli fragmentace a hmotnostní spektrum nyní obsahuje jen signál intaktního proteinu. V naší dosavadní metodě docházelo k mírné fragmentaci, která se projevovala dodatečnými signály o nízké hmotě v oblasti nízkých m/z. Tato fragmentace pak byla u některých specifických uživatelských vzorků relativně výrazná.

S radostí můžeme oznámit, že HDX-MS robotika je nyní plně funkční. Po důkladném čistění, doplnění všeho spotřebního materiálu (objednávka jehel do robota trvala 7 měsíců...) a kompletní kalibraci a odladění máme plní funkční automatizaci přípravy HDX-MS vzorků od labellingu pomocí D2O přes quenching až po digestion a LC-MS analýzu.
Modifikovali jsme řadu kroků původní instrumentační metody na ovládání robota a získali jsme tak výrazně lepší reprodukovatelnost dat oproti původní Waters metodě se kterou je robot dodáván.
Další upgrade, který jsme zavedli paralelně s robotem, je nová metoda akvizice (tzv. HDX-DIA) a díky ní možná automatická validace všech HDX-MS dat, což je v současné době na tomto poli hlavní bottleneck.
Pomocí kombinace cyklické iontové mobility, MSe DIA akvizice dat a špičkového HDX-MS softwaru nyní sbíráme a analyzujeme kvalitní data ve dvou dimenzích, jak MS1 (celé hmoty peptidů) tak MS2 (fragmentace peptidů a MS analýza vznikajících fragmentů), což nám umožňuje automatickou validaci identity a hodnoty deuterace všech peptidů. To zkracuje dobu nutnou pro analýzu dat z typických dnů až týdnů manuální práce na jednotky hodin počítačového procesování. Náš HDX-MS throughput se tak nyní zvýšil zhruba trojnásobně!
Připravujeme nyní na náš nový přístup s iontovou mobilitou a MSe akvizicí metodickou publikaci a za dva týdny ho prezentujeme na HDX-MS 2026 konferenci ve Strasbourgu.
František Filandr
Tereza Nešporová


